【背景及概述】[1][2]
苯丙氨酸即D,L – α- 氨基β – 苯基丙酸,为白色或无色片状晶体,斜方晶系,具有苦杏仁味,水中溶解度29. 6 g/L (25 ℃),微溶于醇,不溶于乙醚,熔点283 ℃。最早由Schulze 于1879 年从羽扇豆幼苗中发现和分离。接着Fischer 于20 世纪初从动物性蛋白质中成功分离得到。苯丙氨酸是一种重要的医药和食品添加剂,属人体必需的八大氨基酸之一。20 世纪80 年代以来,随着抗癌药物制剂和氨基酸输液的发展以及低热量甜味剂阿斯巴甜产量的迅速增加,苯丙氨酸的市场需求增长较快。据统计,1981 年世界L-苯丙氨酸的消费量为50t/a,1990 年增长到9000t/a,1997 年达到1.1 万t/a 左右,2006 年已达到10 万t/a 左右。随着人们生活水平的不断提高,医药保健事业不断发展,我国医药保健品、食品添加剂、饲料添加剂等对苯丙氨酸的需求量正迅速扩大,尤其以氨基酸输液、各种品牌的氨基酸胶囊、氨基酸添加剂、氨基酸为原料的甜味剂等发展最快,需求量最大。随着国内市场的进一步开放和人民生活水平的提高,这种低热量的甜味剂在国内的市场也日益增加,因此,市场对苯丙氨酸的需求也持续增长。
【应用】[1]
1.高效甜味剂—阿斯巴甜
从世界范围来看,苯丙氨酸的主要用途就是生产阿斯巴甜。阿斯巴甜亦称天冬甜素,国内俗称蛋白糖,是一种优良的低热量甜味剂,甜味与蔗糖相似,甜度为蔗糖的200 倍,是目前国际市场上的主导甜味剂。1974 年阿斯巴甜首次被用作甜味剂; 1981 年FAO和WHO 建议阿斯巴甜的摄入量为40mg/人·日,同期美国的相关规定为50mg/人·日。1996 年美国允许阿期巴甜作为一般的甜味剂应用于没有特别规定的所有食品。阿斯巴甜在中国的生产与应用刚刚起步,发潜力大。20 世纪80 年代末,中国就开始研究阿斯巴甜,但由于当时国内没有L- 苯丙氨酸生产装置,进口原料价格昂贵,导致生产成本无法同进口产品竞争,所以没有形成工业化生产,市场供应数量有限。目前,中国每年需消耗蔗糖760 万t/a,若其中的5%由阿斯巴甜来代替,即需阿斯巴甜约1600t/a。相应地,对L- 苯丙氨酸的需求也将随之增长。
2.医药领域
根据在医药领域的不同用途,苯丙氨酸有医药级、食品级、饲料级等不同等级,各等级间的价格差别较大,从18 美元/kg 到40 美元/kg 不等。苯丙氨酸除了直接用于医用复合氨基酸输液和合成医药外,还可用来配制医药的培养介质。用苯丙氨酸合成的医药有HIV 蛋白酶抑制剂、凝乳酶、抗肿瘤药物对氟苯丙氨酸、脑神经传递素等。苯丙氨酸在该领域的消费需求发展平稳增长。
3. 其他领域
近年来,苯丙氨酸的应用领域还在不断拓展,如开发了以苯丙氨酸及其衍生物为原料合成手性中间体技术,发现在未焙烤的可可中加入苯丙氨酸、亮氨酸和降解糖,可显著提高低品质可可的风味等。
【生物代谢】[3]
苯丙氨酸是人体的必需氨基酸,人体本身无法合成,只能由植物和微生物合成。苯丙氨酸合成的起始物为五碳糖磷酸途径的中间产物赤藓糖- 4 – 磷酸(erythrose – 4 – phosphate ,E4P )和糖酵解过程的中间产物磷酸烯醇式丙酮酸(phophoenolpyruvate ,PEP )二者缩合形成一个七碳酮糖开链磷酸化合物称为3 – 脱氧- α- 阿拉伯庚酮糖酸-7 -磷酸(DAHP ),然后DAHP 转化为莽草酸(SHIK ),然后再转化为分支酸(CHA ),由分支酸合成苯丙酮酸(PPY ),最后苯丙酮酸经转氨作用生成苯丙氨酸,见图:
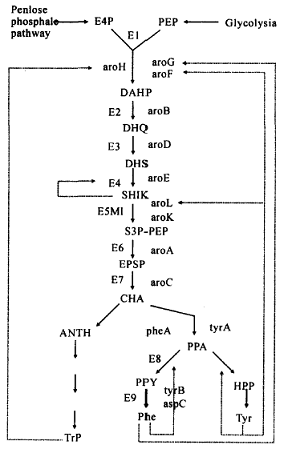
【制备】[3]
1.提取法
提取法是指以天然产物为原料,通过分离纯化等方法生产苯丙氨酸的方法。工业上将脱脂大豆用盐酸水解后,除去酸性氨基酸,用活性炭或脱色树脂吸附苯丙氨酸和酪氨酸,然后使用溶剂将苯丙氨酸溶出,分离。另一种方法是将脱脂大豆用盐酸水解液中苯丙氨酸转变为2 ,5 -二溴苯磺酸盐,然后利用溶解度的差异从其它氨基酸中分离出来。该工艺较复杂,分离提取困难,产品质量不稳定,生产成本较高。另外,还可以以猪毛等为原料生产,但产酸率低,投资大,能耗大,原料来源有限,产量不易扩大。
2. 化学合成法
1)苯甲醛与乙酰甘氨酸缩合法
一般先将甘氨酸乙酰化,获得乙酰甘氨酸,再与苯甲醛缩合成乙酰氨基肉桂酸内酯,后者经水解、电解、还原、酶水解,即得到苯丙氨酸。该方法合成苯丙氨酸原料易得、成本较低,但工艺路线长、步骤多,收率较低。
2)氰氨法
早在1951 年采用氰氨法制备苯丙氨酸,但化学产率及放化产率都仅在28 %左右。1978 年又采用C6H5CH214CN 为原料,由于放化合成步骤(包括从K14CN 制备C6H5CH214CN的放化合成)长,收率仍低于60 %。在此方法上进行改进,以C6H5CH2CHO 为原料制备D,苯丙氨酸-1 -14C,化学产率和放化率都达到67 %。然后嗜热菌蛋白酶通过酶促由DL-苯丙氨酸-1-14 C 与Z-L-丙氨酸合成Z – L-Ala-L-Phe-OM (1-14C )二肽,达到消旋苯丙氨酸的拆分,再将二肽用嗜热菌蛋白酶在N – 甲基吗啉缓冲溶液中进行酶促反应,最终获得苯丙氨酸。该方法在引入K14CN以及随后的三步反应中条件较温和,终产物得率和纯度均较高。缺点是由于反应过程中引入剧毒物K14CN ,三废处理困难。
3)甘氨酸法
甘氨酸法需要先对甘氨酸的羧基和氨基进行保护,生成苯亚甲氨基乙酸乙酯。再利用α- 亚甲基的氢原子的活泼性,使之在相转移条件下进行烷基化反应。最后,经水解反应,制得DL – 苯丙氨酸。该法反应条件温和、原料易得、收较高、无剧毒原料、无难以处理的三废问题,所用的有机溶剂可以回收,是一条很有发展前途的化学合成方法。
3. 微生物发酵法生产苯丙氨酸
1)使用酵母菌生产
从天然环境中分离到一株具有较高苯丙氨酸氨解酶(PAL )活性的菌株,以此为出发菌株进行UV 和EMS 诱变处理,所得菌株较原菌株酶活力有较大提高,且该菌在中试中生长良好,累计产量达58. 0 g L -1 。
2)使用杆菌生产 苯丙氨酸
由短杆菌变异株FMP92814 出发对其产苯丙氨酸条件进行了优化。通过人工诱变选育所获得的乳糖发酵短杆菌FMP92814可利用较粗放的农副产品,淀粉水解糖、玉米糖浆、豆饼粉水解液、糖蜜作原料发酵生产苯丙氨酸,可以降低生产成本,适合目前各氨基酸发酵厂推广。
3)使用假单胞菌生产苯丙氨酸
将从土壤中筛选假单胞菌(Pseudomonas sp. )E4 -106 株细胞进行了 苯丙氨酸生产实验。结果显示转氨反应最适温度35~40 ℃;在pH7~pH10 内催化反应而活力变化不大;表面活性剂处理细胞或在反应液中加入Mg2 +能显著提高转氨反应速度。在此反应体系中,E4 – 106 菌株单位湿重细胞的转氨酶活力为1039U /g ;当产物苯丙氨酸质量浓度为32. 2 g/L和50. 4 g /L时,苯丙酮酸摩尔转化率分别为97. 5 %和87. 2 %,产物回收率为81. 8 %。
3.酶法生产L – 苯丙氨酸
酶法生产具有产物浓度高、纯化步骤少、生产能力强等优点,缺点是部分原料成本高。专家们认为由苯甲醛→海因→苯丙酮酸→苯丙氨酸或由苯甲醛→肉桂酸→苯丙氨酸的路线是最佳方案。
1)一酶一酸法
一酶一酸法即以海因为原料苯丙酮酸酶法,自上世纪80 年代末就开始了该方法工业化开发研究,

2)两菌两酶法
通过两菌双酶法利用大肠杆菌EP8-10 经培养后产生高活力转氨酶和低活力的天冬氨酸酶,而E. coli EA则产生高活力天冬氨酸酶和很低的转氨酶,耦合EP8 – 10 中转氨酶和EA – 1中Asp 酶作用,由苯丙酮酸和富马酸生成L- Phe ,该体系最佳条件为:EA-1 和EP8 – 10 两种细胞质量比为0. 6∶1 ,n (PPA )/n (Fu ) =1∶1. 2 (摩尔比)。当PPA 浓度为0. 24 mol/ L时,反应6 h,可生成38. 5 g/ L 苯丙氨酸。
5. 基因工程法生产L-苯丙氨酸
苯丙氨酸合成途径有多个调控位点,图中的DAHP 合成酶(DS )、分枝酸变位酶(CM )和预苯酸脱水酶(PD )是受调控的关键酶;转氨酶(AT )则是合成途径中最后一步催化苯丙酮。

【主要参考资料】
[1] 邓菊香, 王祖元. 苯丙氨酸的生产现状与发展前景[J]. 安徽化工, 2007, 33(4): 1-3.
[2] 李永辉, 刘云, 徐琪寿. 苯丙氨酸生物合成的研究进展[J]. 生物技术通讯, 2002, 13(4): 296-300.
[3] 李冀新, 张超. L-苯丙氨酸生产及应用研究进展[J]. 氨基酸和生物資源, 2006, 28(2): 51-56.



 微信扫一扫打赏
微信扫一扫打赏
